Технический прогресс в производстве вакцин должен сократить время до проведения клинических испытаний, сдвинув с мертвой точки тестирование перспективных новых вакцин.
За последнее десятилетие исследования в области ВИЧ привели к появлению многих перспективных идей по разработке вакцин для профилактики СПИДа, но только некоторые вакцины были протестированы в клинических испытаниях.
Одной из причин является техническая сложность изготовления вакцин на основе белков оболочки вируса, объясняет Фил Берман, который вел разработку основного компонента вакцины, показавшей определенную эффективность против ВИЧ в клинических испытаниях. Об этом пишет Sciencedaily.

Фил Берман
Фил Берман, профессор биомолекулярной инженерии при Калифорнийском университете Санта-Крус, в настоящее время разработал новые методы для производства вакцин против ВИЧ. Его подход решает основные технические проблемы, которые сбили с толку ученых в данной области.
«Было описано несколько десятков интересных вакцин-кандидатов, но большинство из них не было протестировано на людях, потому что раньше не было возможности производить их доступным и своевременным образом», – сказал Берман. «Технология, которую мы разработали, должна сдвинуть с мертвой точки разработку вакцины против ВИЧ, поскольку она значительно сокращает время, улучшает результат и снижает затраты».
Лаборатория Бермана смогла использовать робототехнику, чтобы сократить время, необходимое для создания стабильных клеточных линий, которые нужны для производства белков для вакцины, и в то же время значительно увеличить количество белка, который могут вырабатывать клеточные линии.
Усовершенствованный результат позволяет уменьшить размер биореактора, необходимого для производства вакцины для крупных клинических испытаний – от 200- до 10000-литровых сосудов до 50- или 100-литровых сосудов, что приводит к огромной экономии необходимого оборудования и стоимости материалов. Кроме того, лаборатория Бермана смогла создать клеточные линии, которые производят белки оболочки ВИЧ, связанные с подходящим видом углеводных компонентов (называемых гликанами), необходимых для эффективного иммунного ответа.
«Углеводы, связанные с белком, действительно важны, это то, что никто не понимал до недавнего времени», – сказал Фил Берман. «Традиционный способ создания вакцин на основе белков оболочки включал в себя неправильный вид углеводов».
Клеточные линии, полученные из овариальных клеток китайского хомячка (СНО), являются промышленным стандартом, используемым для получения сложных рекомбинантных белков для терапевтического использования. Эти клетки также используемы для производства вакцин против ВИЧ. Ген для желаемого белка переносится в клетки СНО во время процесса, называемого трансфекцией, и десятки тысяч трансфицированных клеток подвергаются скринингу, чтобы найти несколько редких клеток, которые вырабатывают большие количества белка.
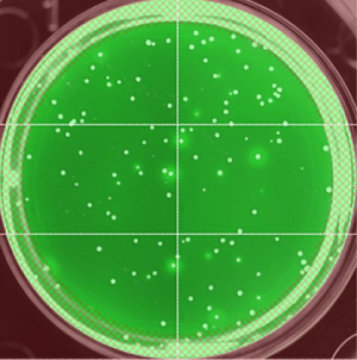
Флуоресцентные антитела использовали для маркировки белка gp120 ВИЧ и идентифицировали высокопродуктивные клеточные линии. Credit: Phil Berman, UCSC
Лучшие клеточные линии выращивают крупными партиями в процессе, подобном дрожжевой ферментации для приготовления пива. Затем белки выделяют и очищают.
Лаборатория Бермана разработала новый роботизированный метод для выделения высокопроизводительных клеточных линий, вырабатывающих белки оболочки ВИЧ. Это сократило время, необходимое для создания стабильных клеточных линий от 18-24 месяцев до 2-3 месяцев при одновременном увеличении результативности со 100 до 200 раз. Данные улучшения указаны по сравнению с предыдущим опытом Бермана во время создания вакцины AIDSVAX, сначала в Genentech, а затем в VaxGen.
AIDSVAX был одним из компонентов экспериментального режима вакцины, используемого в крупномасштабном клиническом исследовании, известном как RV144, который показал 31 %-ную эффективность по предотвращению новых случаев ВИЧ-инфицирования. Результаты RV144 показали, что защита коррелирует с антителами к определенному сегменту белка оболочки ВИЧ, называемого gp120.
Другое исследование, однако, показало, что многие из наиболее высокоактивных антител (широко нейтрализующих антител, способных нейтрализовать разные штаммы ВИЧ) фактически распознают углеводные компоненты (гликаны), присоединенные к gp120.
«Мы поняли, что первоначальная вакцина против СПИДа AIDSVAX имеет совершенно неправильный тип углеводов и что мы могли бы повысить уровень защиты, если бы смогли найти способ сделать это с соответствующим типом углеводов», – сказал Фил Берман.
Поэтому Берман и аспирант Габриэль Бирн решили создать клеточную линию, которая смогла бы выработать нетипичные гликаны, обнаруженные на белках оболочки ВИЧ, скорее, чем комплексные гликаны, которые как правило производят клетки СНО.
Это стало возможным благодаря мощной новой технологии редактирования генов, известной как CRISPR / Cas9. Лаборатория Бермана использовала CRISPR для создания новой клеточной линии под названием MGAT CHO, которая вырабатывает белки, не содержащие комплексные гликаны (с сиаловой кислотой) и которые обогащены простым видом гликанов с высоким содержанием маннозы, обнаруженным на белках оболочки ВИЧ.
Неожиданным преимуществом этой новой клеточной линии было то, что она обеспечивала более простой и менее дорогостоящий процесс восстановления и очистки белков.
«Люди привыкли думать, что углеводы не являются иммуногенными, но ВИЧ переворачивает все с ног на голову, и оказывается, что самые важные антитела связаны с данным нетипичным углеводом», – сказал Берман. «Мы теперь создали усовершенствованную версию вакцины, используемую в исследовании RV144. Надеемся, что она повысит эффективность с 31 процента до более чем 50 процентов, то есть до уровня, необходимого для регистрации продукта».
Лаборатория Бермана в настоящее время имеет две клеточные линии и, по его словам, они готовы начать производство вакцин в больших масштабах. Сейчас он ищет партнеров и источники финансирования, чтобы протестировать вакцины в условиях клинических испытаний. Одна вакцина является улучшенной версией AIDSVAX, которая включает правильный тип гликанов. Другая вакцина сделана из штамма вируса, который известен как Clade C и который широко распространен в Южной Африке и Индии и составляет большинство новых случаев ВИЧ-инфицирования во всем мире.
Исследователи продолжительно использовали вакцину AIDSVAX в клинических исследованиях, потому что было очень сложно создать новые вакцины против ВИЧ, сказал Берман, отметив, что таких исследований было 14 со времен выпуска результатов RV144 в 2009 году. «Они до сих пор используют ту же старую вакцину, которую мы произвели в начале 1990-х годов. Хоть стабильность и безопасность продукта свидетельствуют о качестве вакцины, которую мы сделали, необходимы новые вакцины, которые проявят максимальную эффективность», – подчеркивает Берман. «Необходимо найти более эффективный способ вакцинации против ВИЧ».


 ПОИСК ПО САЙТУ
ПОИСК ПО САЙТУ  поиск по ресурсному центру
поиск по ресурсному центру 



